
2月26日晚間,百濟神州發布2025年度業績快報:2025年營收382.05億元,同比上升40.4%,歸屬于母公司所有者的凈利潤14.22億元,扭虧為盈。
2025年,百濟神州產品收入為377.70億元,同比上升39.9%,上年同期產品收入為269.94億元,產品收入的增長主要得益于百悅澤(澤布替尼),以及安進公司授權產品和百澤安?(替雷利珠單抗)的銷售增長。
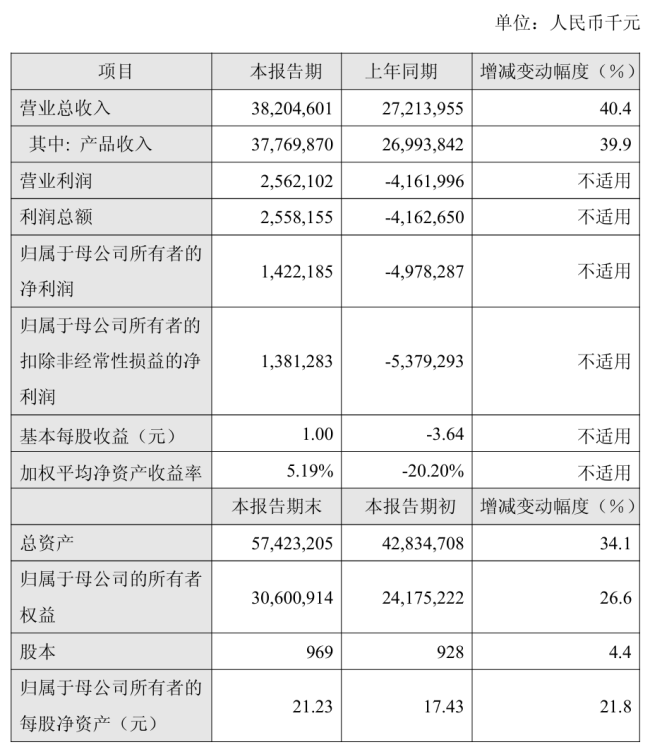
來源:上市公司公告
據動脈網梳理,這是百濟神州2014年至今12年來首次實現全年盈利。
這份業績快報的意義遠超“扭虧為盈”本身,過去市場對百濟神州的疑慮多集中在“何時盈利”,2025年或許正是百濟神州完成“自我造血”的關鍵一躍。
然而二級市場的表現似乎有些“反差”:2月26日和27日,百濟神州A股分別下跌5.65%和2.18%,港股下跌9.16%和1.08%。美股在2月26日(當地時間)下跌8.48%。
動脈網從多位醫藥領域業內人士處了解到,一方面,百濟神州二級市場的變動可能與2026年業績預測有關,營收增速有所放緩,市場或許會擔心核心大單品是否已接近峰值;另一方面,可能市場情緒已經有所提前消耗,也可能與匯率有關。
根據公告,百濟神州預測2026年營收約436億元至450億元,與2025年相比,營收增速約14.12%-17.79%,毛利率為80%區間,營收扣除經營成本費用后約46億元至53億元。
12年來首次實現全年盈利
百濟神州成立于2010年,并于2016年、2018年先后登陸納斯達克、港交所,2021年12月,又在上海證券交易所科創板上市。
根據Wind數據,2014至2025年,百濟神州營收持續高速增長,從2014年的約8900萬元一路躍升至2025年的382.05億元。
尤其在2021年及以后,營收增速顯著加快且較為穩定,2023年突破170億元,2024年達到272.14億元,2025年更是逼近400億元大關,營收擴張能力強勁。
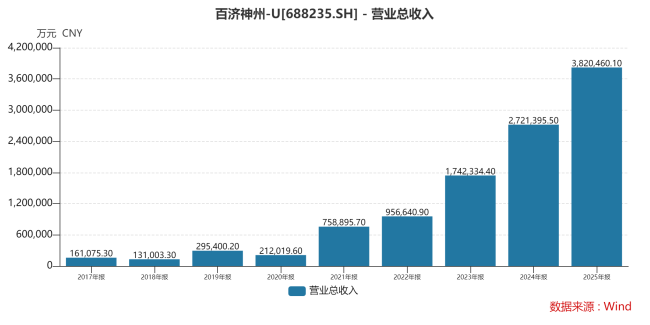

來源:Wind
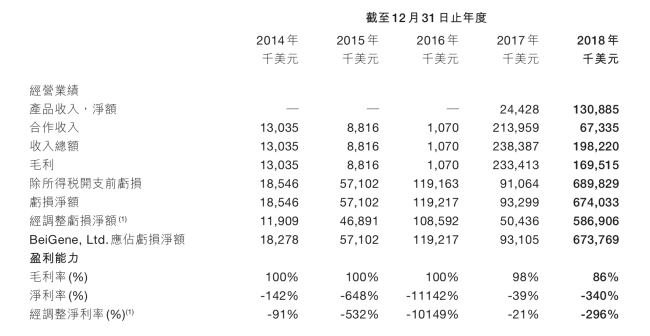
來源:百濟神州2018年財報
然而與營收的持續增長形成鮮明對比的是,百濟神州在長達八年的時間里持續處于虧損狀態。
結合Wind數據和百濟神州財報,2014年至2024年,百濟神州歸母凈利潤均為負值,且虧損額整體呈擴大趨勢,2022年虧損擴大至136.42億元,創下虧損峰值,此后虧損有所收窄,但2024年仍虧損49.78億元。
轉折點出現在2025年,首次實現全年歸母凈利潤為正,達到14.22億元——在持續高投入和快速擴張之后迎來盈利拐點。
根據公告,2025年扭虧為盈和營收增長的原因主要包括三方面:
一是BTK抑制劑澤布替尼,堪稱百濟神州當前主要現金牛與護城河。2025年澤布替尼全球銷售額總計280.67億元,同比增長48.8%,已在BTK抑制劑領域穩固確立全球領導者的地位。
美國仍是澤布替尼最大的商業化市場,銷售額總計202.06億元,同比增長45.5%;歐洲銷售額總計42.65億元,同比增長66.4%;中國銷售額總計24.72億元,同比增長33.1%。
澤布替尼是全球獲批適應癥最廣泛的BTK抑制劑,同時也是唯一一款給藥靈活,可每日一次或每日兩次的BTK抑制劑。
二是抗PD-1藥物替雷利珠單抗,2025年全球銷售額總計52.97億元,同比增長18.6%,是百濟神州實體瘤產品組合的基石產品,已在多種腫瘤類型和疾病領域中顯示出潛力。
三是2025年安進公司授權許可產品銷售額為34.71億元,同比增長33.6%。據了解,2019年10月,百濟神州與安進公司曾建立全球腫瘤戰略合作關系,將共同開發20款安進抗腫瘤藥物。
在百濟神州業績增長背后,可以看到收入增長幾乎完全由產品收入驅動,而非一次性授權費用——2025年的377.70億元產品收入占總營收98.9%。
跨越盈虧線后,百濟神州下一步如何走
對于百濟神州能否從2025年開始維持每年盈利,首先需要關注其全球市場開發能力,在國內市場競爭日趨激烈之時,國際市場的潛力尤為重要。
根據公告,2025年澤布替尼的境外收入為255.95億元,占澤布替尼總收入91.2%,以此計算,百濟神州2025年全年境外收入占比至少為67%,境外收入比例進一步提高——2024年境外收入占比為62.85%。
百濟神州的產品開發一直立足全球市場。
其中澤布替尼目前已在全球超過75個市場獲批,臨床開發項目迄今已在全球超過30個國家和地區開展超過45項試驗,入組超過7900例患者。
而且澤布替尼“頭對頭”對比伊布替尼的相關全球臨床3期ALPINE試驗展示出持續的無進展生存期(PFS)獲益,且心血管事件發生率較低。
替雷利珠單抗目前已在全球超過50個市場獲批,臨床開發項目迄今已在全球超過33個國家和地區入組超過15800例受試者。
百濟神州預計將于2026年上半年在美國和中國遞交替雷利珠單抗聯合百赫安?(澤尼達妥單抗)用于HER2陽性GEA成人患者一線治療的新增適應癥上市許可申請,并有望于2026年下半年在日本獲得替雷利珠單抗用于胃癌(GC)成人患者一線治療的監管決定。
再從產品管線來看,據梳理,百濟神州已構建覆蓋血液瘤及肺癌、消化道腫瘤和乳腺癌等實體瘤領域的多元管線,涵蓋小分子、單抗、雙抗/多抗、蛋白降解(CDAC)、ADC、細胞與基因治療(CGT)等藥物模式。
目前百濟神州已有超過80個臨床前項目正在推進,多款處于臨床后期階段的產品已臨近商業化。
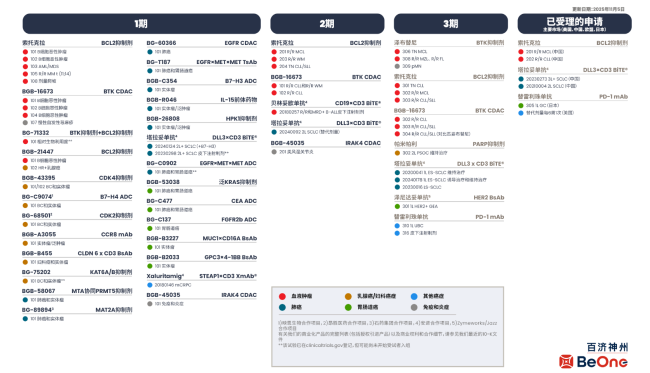
百濟神州全球自主研發和合作管線(截至2025年11月5日) 來源:百濟神州官網
在血液腫瘤領域,百濟神州新一代BCL2抑制劑索托克拉(百悅達?)尤其值得關注,該藥物于2026年1月上市,從遞交NDA到獲批僅用8個月,用于治療慢性淋巴細胞白血病(CLL)/小淋巴細胞淋巴瘤(SLL)及套細胞淋巴瘤(MCL),成為國內首款且唯一可用于治療MCL的BCL2抑制劑。
據了解,套細胞淋巴瘤患者的總體生存時間仍然較短,常規化療5年生存率不足30%,且有效維持時間短,患者生存時間10年以上的僅占8%。套細胞淋巴瘤患者以老年男性為主,且多數在診斷時已處于疾病晚期,復發難治以及伴有高危因素的患者常規治療療效有限,是長期存在的臨床挑戰。
與此同時,索托克拉已獲得FDA授予的優先審評資格,用于治療(R/R)MCL成人患者,且已在歐盟遞交用于治療(R/R)MCL成人患者的上市許可申請。百濟神州已完成索托克拉聯合澤布替尼作為固定療程方案對比阿可替尼聯合維奈克拉用于治療初治CLL成人患者的3期試驗首例受試者入組。
百濟神州預計將于2026年上半年獲得美國FDA對索托克拉單藥用于治療(R/R)MCL成人患者新藥上市申請的監管決定,并預計將于2026年下半年啟動索托克拉用于治療多發性骨髓瘤成人患者的3期試驗。
在實體瘤管線方面:
●針對乳腺癌與婦科癌癥,百濟神州已啟動BG-75202(KAT6A/B抑制劑)以及BG-75908(CDK2CDAC)的首次人體試驗。
●針對肺癌,百濟神州已啟動BG-C0902(EGFRxMETxMET抗體偶聯藥物)的首次人體試驗。
●針對胃腸道癌,BGB-B2033(GPC3×41BB雙特異性抗體)獲得FDA快速通道資格認定,用于治療接受全身治療期間或之后出現疾病進展的肝細胞癌成人患者。
在炎癥和免疫治療領域,百濟神州預計將于2026年上半年對BGB-16673(BTKCDAC)治療中重度慢性自發性蕁麻疹成人患者的1b期試驗進行數據讀出。
綜上所述,2025年的盈利標志著百濟神州正式跨越了創新藥企最艱難的“盈虧平衡點”。從澤布替尼的全球突圍到索托克拉的接棒上市,百濟神州用9年長跑證明了中國藥企有能力在全球市場實現自我造血。
然而盈利只是起點,如何將深厚的管線儲備持續轉化為現金流,或許是其下一階段的關鍵考驗。
富騰優配提示:文章來自網絡,不代表本站觀點。